¿Qué es el diagrama de Moeller y cómo funciona?


Escrito y verificado por la psicóloga Valeria Sabater
El diagrama de Moeller es un recurso útil tanto para los ingenieros químicos como para los estudiantes de esta disciplina. Lo que hace es proporcionarte una representación visual de las estructuras moleculares para saber cómo se unen entre sí los propios átomos. Esta conjunción es la que termina formando un espacio tridimensional.
Bien es cierto que, a simple vista, parece una materia algo compleja. Sin embargo, no deja de ser un tema fascinante. Gracias a esta herramienta —que cuenta ya con más un siglo de antigüedad— se calcula la configuración electrónica de los átomos de un modo sencillo y, sobre todo, visual. Esa es su mayor ventaja. A continuación, te ofrecemos todos los datos.
Diagrama de Moeller: qué es y para qué sirve
El diagrama de Moeller es un gráfico que sirve para calcular la configuración electrónica de un átomo mediante su número atómico (Z). En caso de que estudies química, esta herramienta te facilitará el comprender mejor las propiedades elementales de las sustancias, así como sus reacciones. También a memorizar de forma sencilla su estructura.
Este recurso, también conocido como «método de la lluvia» o «regla de las diagonales», fue creado por el físico alemán Erwin Madelung en 1881. Para comprenderlo, es necesario profundizar en el principio que este mismo científico formuló y que conocemos como «regla de Madelung». Toma nota de las utilidades que presenta este patrón.
Determinar la configuración electrónica de un elemento químico
Un libro canónico para muchos estudiantes y que profundiza, tanto en este recurso como en las diferentes parcelas de esta disciplina, es Química orgánica (2013), de Robert Neilson Boyd y Robert T Morrison. La principal ventaja que obtendrás con esta regla es establecer el orden en el que se llenan los orbitales atómicos de un elemento químico.
Todo esto te permite, poco a poco, vislumbrar su configuración electrónica y detectar la geometría tridimensional de una molécula, así como la disposición de sus átomos. De ese modo, comprenderás mejor las propiedades químicas y físicas de sustancias como el oxígeno, el calcio, zirconio, etc.
Gracias a esta herramienta el desarrollo de la química avanzó y se crearon grandes desarrollos tecnológicos. Asimismo, entre sus utilidades están también las siguientes:
- Predecir las propiedades químicas de un elemento.
- Clarificar el grupo y período de un elemento en la tabla periódica.
- Profundizar en las reacciones químicas de los elementos atendiendo a su naturaleza atómica.
Entender los enlaces químicos
Si te preguntas para qué es útil el diagrama de Moeller, entre una de sus finalidades está el comprender los enlaces químicos de cada configuración electrónica. Al detectar esta característica, se puede determinar incluso la distribución de carga y la polaridad de la molécula.
Algo así es muy útil en el campo de la ingeniería y para el desarrollo de diferentes maquinarias, como sistemas de refrigeración, calefacción y hasta diseñar dispositivos de previsión meteorológica.
La regla de Madelung
A la hora de llevar a cabo un patrón de Moeller es esencial comprender la regla de Madelung. La revista Inference International Review of Science profundiza en su trascendencia en el campo de las ciencias naturales. Lo que te permite este principio químico es determinar el orden en que los electrones llenan los orbitales atómicos en un átomo o ion. Veamos más datos:
- La regla de Aufbau: la primera regla de Madelung establece que los electrones llenan primero los orbitales más bajos en energía antes de ocupar los orbitales más altos. En otras palabras, los orbitales de menor nivel de energía se llenan antes.
- Regla de Hund: la segunda regla te dice que, cuando se llenan los orbitales de un mismo subnivel, los electrones ocupan cada orbital con espines paralelos antes de emparejarlos. Esto minimiza la repulsión electrónica y, por lo tanto, la energía del sistema.
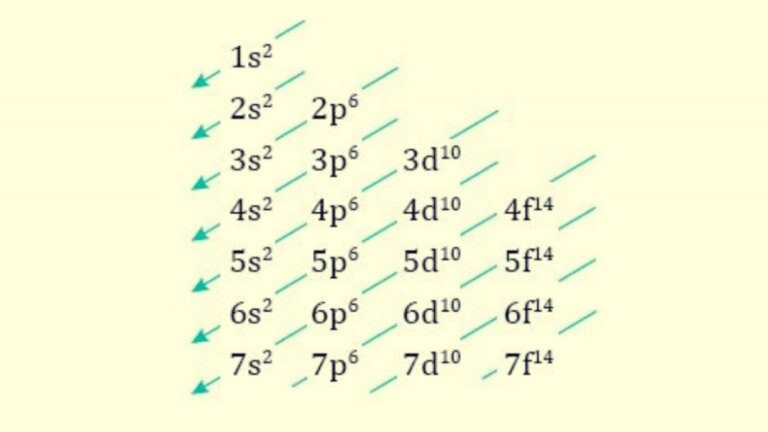
- La secuencia de la que parte: el principal objetivo de la regla de Madelung es que te facilita determinar la secuencia de llenado de los orbitales atómicos. Lo hace siguiendo una secuencia muy concreta basada en la energía de los subniveles. Es la siguiente: 1s, 2s, 2p, 3s, 3p, 4s, 3d, 4p, 5s, 4d, 5p, 6s, 4f, 5d, 6p, 7s, 5f, 6d, 7p.
¿Cómo llevar a cabo la representación gráfica de Moeller?
Llega el momento más decisivo. Para llevar a cabo tu patrón de Moeller debes crear una tabla en la que aparezcan los elementos clave que lo conforman. Aunque lo parezca, no es difícil. Tiene su lógica. Una vez comprendes los elementos que la integran podrás descubrir, poco a poco, la configuración electrónica de un átomo. Estos son los pasos:
Elementos del gráfico
- Niveles principales: parten del número cuántico (n) en la columna izquierda del esquema y se organizan de menor a mayor en forma descendente.
- Orbitales atómicos: se ordenan siempre según su forma y se identifican por las letras «s», «p», «d» y «f».
- Subniveles: hacen referencia a los números ubicados en el lado derecho de la tabla. Ten en cuenta que un nivel suele tener, por término medio, varios subniveles.
- Los trazos diagonales: son las flechas que interceptan los subniveles. Empiezan por el más pequeño (1s), desde arriba hacia abajo y de derecha a izquierda.
Pasos básicos para su realización
- Buscar el número atómico: hay que empezar clarificando el elemento en la tabla periódica. El número atómico hace referencia a la cantidad de protones que tiene el núcleo de un átomo.
- Dibujar el patrón de Moeller: traza el gráfico con tantos círculos como electrones tenga el elemento. Recuerda que el número de electrones de un átomo es igual al número atómico.
- Aplica la regla de Madelung: empieza poniendo los electrones en los orbitales más bajos, de acuerdo con la regla de Madelung que antes te hemos descrito. Recuerda que este principio establece el orden en el que se van llenando los orbitales atómicos.
- Colocación de los orbitales: el próximo paso es seguir situando los electrones en los orbitales siguientes, hasta que todos y cada uno hayan sido asignados.
Ejemplos y excepciones
El diagrama de Moeller se aplica en la gran mayoría de los elementos de la tabla periódica. Pero cuidado, porque hay excepciones y, ejemplo de ello, son los metales de transición, así como ciertos elementos de número atómico elevado que incumplen el principio de Aufbau. A continuación, te damos un ejemplo de cada uno de ellos.
Ejemplo 1: Oxígeno (Z = 8)
- El diagrama de Moeller del oxígeno es el siguiente: 1s² 2p⁶.
- En este caso, puedes ver que el oxígeno tiene 8 electrones, por lo que el diagrama presentaría 8 círculos. Los primeros 2 electrones se colocan en el orbital 1s y los siguientes 6 electrones se colocan en el orbital 2p.
Ejemplo 2: Hidrógeno (Z = 1)
- El patrón de Moeller del hidrógeno se conforma de esta manera: 1s¹.
- El hidrógeno tiene 1 electrón, por lo tanto, el diagrama tiene 1 círculo. El electrón se coloca en el orbital 1s.
Ejemplo 3: Calcio (Z = 20)
- En este caso, el diagrama Moeller del calcio tiene un patrón un poco más complejo: 1s² 2s² 2p⁶ 3s² 3p⁶.
- Como puedes apreciar, el calcio presenta 20 electrones, por lo que el patrón se representaría con 20 círculos. Los primeros 10 electrones se colocan en los orbitales 1s, 2s, y 2p. Los siguientes 10 electrones van en los orbitales 3s y 3p.
Excepciones
- El cromo (Z = 24): tiene una configuración electrónica de 1s² 2s² 2p⁶ 3s² 3p⁶ 4s¹ 3d⁵. Según la regla de Madelung, el cromo debería tener el siguiente patrón: 1s² 2s² 2p⁶ 3s² 3p⁶ 4s² 3d⁴. No obstante, la configuración real del cromo tiene un electrón en el orbital 4s, en lugar de en el orbital 3d.
- El níquel (Z = 28): su representación sería la siguiente; 1s² 2s² 2p⁶ 3s² 3p⁶ 4s² 3d⁸. Tal y como explica la norma de Madelung, su organización electrónica debería ser de 1s² 2s² 2p⁶ 3s² 3p⁶ 4s¹ 3d⁷. Pero en realidad, presenta tiene 8 electrones en la subcapa 3d, en lugar de 7 electrones.
- El cobre (Z = 29): se organiza del siguiente modo: 1s² 2s² 2p⁶ 3s² 3p⁶ 4s¹ 3d¹⁰. En este caso, sucede lo mismo que en los anteriores. No encaja. Su simbolización electrónica real tiene 10 electrones y no 9 electrones.
La herramienta de Moeller, un instrumento de valor
El gráfico de Moeller es una herramienta útil para visualizar y comprender la organización de los electrones en un átomo. Podríamos definirla como un recurso valioso para la ciencia en general y, sobre todo, como una estrategia muy pedagógica en el estudio de la química.
Si te estás iniciando en su comprensión, ten paciencia. Te recomendamos practicar siempre que puedas. Los ingenieros llevan décadas sirviéndose de él para predecir de forma teórica el rendimiento de sistemas e instalaciones. Resulta fascinante saber que muchos de los instrumentos que forman parte de nuestra vida cotidiana, fueron diseñados con esta formulación.
El diagrama de Moeller es un recurso útil tanto para los ingenieros químicos como para los estudiantes de esta disciplina. Lo que hace es proporcionarte una representación visual de las estructuras moleculares para saber cómo se unen entre sí los propios átomos. Esta conjunción es la que termina formando un espacio tridimensional.
Bien es cierto que, a simple vista, parece una materia algo compleja. Sin embargo, no deja de ser un tema fascinante. Gracias a esta herramienta —que cuenta ya con más un siglo de antigüedad— se calcula la configuración electrónica de los átomos de un modo sencillo y, sobre todo, visual. Esa es su mayor ventaja. A continuación, te ofrecemos todos los datos.
Diagrama de Moeller: qué es y para qué sirve
El diagrama de Moeller es un gráfico que sirve para calcular la configuración electrónica de un átomo mediante su número atómico (Z). En caso de que estudies química, esta herramienta te facilitará el comprender mejor las propiedades elementales de las sustancias, así como sus reacciones. También a memorizar de forma sencilla su estructura.
Este recurso, también conocido como «método de la lluvia» o «regla de las diagonales», fue creado por el físico alemán Erwin Madelung en 1881. Para comprenderlo, es necesario profundizar en el principio que este mismo científico formuló y que conocemos como «regla de Madelung». Toma nota de las utilidades que presenta este patrón.
Determinar la configuración electrónica de un elemento químico
Un libro canónico para muchos estudiantes y que profundiza, tanto en este recurso como en las diferentes parcelas de esta disciplina, es Química orgánica (2013), de Robert Neilson Boyd y Robert T Morrison. La principal ventaja que obtendrás con esta regla es establecer el orden en el que se llenan los orbitales atómicos de un elemento químico.
Todo esto te permite, poco a poco, vislumbrar su configuración electrónica y detectar la geometría tridimensional de una molécula, así como la disposición de sus átomos. De ese modo, comprenderás mejor las propiedades químicas y físicas de sustancias como el oxígeno, el calcio, zirconio, etc.
Gracias a esta herramienta el desarrollo de la química avanzó y se crearon grandes desarrollos tecnológicos. Asimismo, entre sus utilidades están también las siguientes:
- Predecir las propiedades químicas de un elemento.
- Clarificar el grupo y período de un elemento en la tabla periódica.
- Profundizar en las reacciones químicas de los elementos atendiendo a su naturaleza atómica.
Entender los enlaces químicos
Si te preguntas para qué es útil el diagrama de Moeller, entre una de sus finalidades está el comprender los enlaces químicos de cada configuración electrónica. Al detectar esta característica, se puede determinar incluso la distribución de carga y la polaridad de la molécula.
Algo así es muy útil en el campo de la ingeniería y para el desarrollo de diferentes maquinarias, como sistemas de refrigeración, calefacción y hasta diseñar dispositivos de previsión meteorológica.
La regla de Madelung
A la hora de llevar a cabo un patrón de Moeller es esencial comprender la regla de Madelung. La revista Inference International Review of Science profundiza en su trascendencia en el campo de las ciencias naturales. Lo que te permite este principio químico es determinar el orden en que los electrones llenan los orbitales atómicos en un átomo o ion. Veamos más datos:
- La regla de Aufbau: la primera regla de Madelung establece que los electrones llenan primero los orbitales más bajos en energía antes de ocupar los orbitales más altos. En otras palabras, los orbitales de menor nivel de energía se llenan antes.
- Regla de Hund: la segunda regla te dice que, cuando se llenan los orbitales de un mismo subnivel, los electrones ocupan cada orbital con espines paralelos antes de emparejarlos. Esto minimiza la repulsión electrónica y, por lo tanto, la energía del sistema.
- La secuencia de la que parte: el principal objetivo de la regla de Madelung es que te facilita determinar la secuencia de llenado de los orbitales atómicos. Lo hace siguiendo una secuencia muy concreta basada en la energía de los subniveles. Es la siguiente: 1s, 2s, 2p, 3s, 3p, 4s, 3d, 4p, 5s, 4d, 5p, 6s, 4f, 5d, 6p, 7s, 5f, 6d, 7p.
¿Cómo llevar a cabo la representación gráfica de Moeller?
Llega el momento más decisivo. Para llevar a cabo tu patrón de Moeller debes crear una tabla en la que aparezcan los elementos clave que lo conforman. Aunque lo parezca, no es difícil. Tiene su lógica. Una vez comprendes los elementos que la integran podrás descubrir, poco a poco, la configuración electrónica de un átomo. Estos son los pasos:
Elementos del gráfico
- Niveles principales: parten del número cuántico (n) en la columna izquierda del esquema y se organizan de menor a mayor en forma descendente.
- Orbitales atómicos: se ordenan siempre según su forma y se identifican por las letras «s», «p», «d» y «f».
- Subniveles: hacen referencia a los números ubicados en el lado derecho de la tabla. Ten en cuenta que un nivel suele tener, por término medio, varios subniveles.
- Los trazos diagonales: son las flechas que interceptan los subniveles. Empiezan por el más pequeño (1s), desde arriba hacia abajo y de derecha a izquierda.
Pasos básicos para su realización
- Buscar el número atómico: hay que empezar clarificando el elemento en la tabla periódica. El número atómico hace referencia a la cantidad de protones que tiene el núcleo de un átomo.
- Dibujar el patrón de Moeller: traza el gráfico con tantos círculos como electrones tenga el elemento. Recuerda que el número de electrones de un átomo es igual al número atómico.
- Aplica la regla de Madelung: empieza poniendo los electrones en los orbitales más bajos, de acuerdo con la regla de Madelung que antes te hemos descrito. Recuerda que este principio establece el orden en el que se van llenando los orbitales atómicos.
- Colocación de los orbitales: el próximo paso es seguir situando los electrones en los orbitales siguientes, hasta que todos y cada uno hayan sido asignados.

Ejemplos y excepciones
El diagrama de Moeller se aplica en la gran mayoría de los elementos de la tabla periódica. Pero cuidado, porque hay excepciones y, ejemplo de ello, son los metales de transición, así como ciertos elementos de número atómico elevado que incumplen el principio de Aufbau. A continuación, te damos un ejemplo de cada uno de ellos.
Ejemplo 1: Oxígeno (Z = 8)
- El diagrama de Moeller del oxígeno es el siguiente: 1s² 2p⁶.
- En este caso, puedes ver que el oxígeno tiene 8 electrones, por lo que el diagrama presentaría 8 círculos. Los primeros 2 electrones se colocan en el orbital 1s y los siguientes 6 electrones se colocan en el orbital 2p.
Ejemplo 2: Hidrógeno (Z = 1)
- El patrón de Moeller del hidrógeno se conforma de esta manera: 1s¹.
- El hidrógeno tiene 1 electrón, por lo tanto, el diagrama tiene 1 círculo. El electrón se coloca en el orbital 1s.
Ejemplo 3: Calcio (Z = 20)
- En este caso, el diagrama Moeller del calcio tiene un patrón un poco más complejo: 1s² 2s² 2p⁶ 3s² 3p⁶.
- Como puedes apreciar, el calcio presenta 20 electrones, por lo que el patrón se representaría con 20 círculos. Los primeros 10 electrones se colocan en los orbitales 1s, 2s, y 2p. Los siguientes 10 electrones van en los orbitales 3s y 3p.
Excepciones
- El cromo (Z = 24): tiene una configuración electrónica de 1s² 2s² 2p⁶ 3s² 3p⁶ 4s¹ 3d⁵. Según la regla de Madelung, el cromo debería tener el siguiente patrón: 1s² 2s² 2p⁶ 3s² 3p⁶ 4s² 3d⁴. No obstante, la configuración real del cromo tiene un electrón en el orbital 4s, en lugar de en el orbital 3d.
- El níquel (Z = 28): su representación sería la siguiente; 1s² 2s² 2p⁶ 3s² 3p⁶ 4s² 3d⁸. Tal y como explica la norma de Madelung, su organización electrónica debería ser de 1s² 2s² 2p⁶ 3s² 3p⁶ 4s¹ 3d⁷. Pero en realidad, presenta tiene 8 electrones en la subcapa 3d, en lugar de 7 electrones.
- El cobre (Z = 29): se organiza del siguiente modo: 1s² 2s² 2p⁶ 3s² 3p⁶ 4s¹ 3d¹⁰. En este caso, sucede lo mismo que en los anteriores. No encaja. Su simbolización electrónica real tiene 10 electrones y no 9 electrones.
La herramienta de Moeller, un instrumento de valor
El gráfico de Moeller es una herramienta útil para visualizar y comprender la organización de los electrones en un átomo. Podríamos definirla como un recurso valioso para la ciencia en general y, sobre todo, como una estrategia muy pedagógica en el estudio de la química.
Si te estás iniciando en su comprensión, ten paciencia. Te recomendamos practicar siempre que puedas. Los ingenieros llevan décadas sirviéndose de él para predecir de forma teórica el rendimiento de sistemas e instalaciones. Resulta fascinante saber que muchos de los instrumentos que forman parte de nuestra vida cotidiana, fueron diseñados con esta formulación.
Todas las fuentes citadas fueron revisadas a profundidad por nuestro equipo, para asegurar su calidad, confiabilidad, vigencia y validez. La bibliografía de este artículo fue considerada confiable y de precisión académica o científica.
- Belokolos, E. D. (2017). Mendeleev table: A proof of madelung rule and Atomic Tietz Potential. SIGMA. Symmetry, Integrability and Geometry: Methods and Applications, 13, 038. https://arxiv.org/abs/1706.02535
- Morrison, T., Neilson, B. (2013). Química orgánica. Addison Wesley Longman
- Scerri, E. (2017). On the madelung rule. Inference International Review of Science, 3(1). https://www.researchgate.net/publication/319450452_On_the_Madelung_Rule
Este texto se ofrece únicamente con propósitos informativos y no reemplaza la consulta con un profesional. Ante dudas, consulta a tu especialista.







