Locus coeruleus: anatomía y funciones

Escrito y verificado por el psicólogo Sergio De Dios González
El locus coeruleus (LC) es uno de los núcleos más pequeños, pero más extensamente proyectados en el cerebro. Aparece citado por primera vez en el material publicado por Vicq-d’Azyr en 1786 (1). Hablamos de una estructura que se encuentra localizada en el tronco del encéfalo.
Así, esta estructura del sistema nervioso es conocida por conectar con muchas otras zonas del cerebro. De manera concreta, el locus coeruleus (LC) es una fuente importante de proyecciones de norepinefrina (NE) en todo el sistema nervioso central.
Así, en 1969 la revista Brain Research publica un artículo (Loizou, 1969) que arroja luz sobre esta estructura cerebral. El autor Loizou confirmó mediante su investigación que, como se pensaba, las proyecciones del LC estaban generalizadas y aparentemente difusas (2).
Anatomía del locus coeruleus
Tras la publicación de este trabajo de Loizou, hubo un esfuerzo considerable dedicado a obtener una caracterización más detallada del locus coeruleus y sus conexiones en el cerebro. Así, la investigación posterior a la publicación de la Brain Research se dedicó fundamentalmente a:
- El rastreo anterógrado y retrógrado del tracto.
- La tinción selectiva de las neuronas y fibras NE utilizando anticuerpos dirigidos contra la enzima sintética NE, dopamina-beta-hidroxilasa (DBH). Así, se confirmó la singularidad del locus coeruleus: se trataba de un grupo compacto de neuronas NE cuyas proyecciones se distribuyen ampliamente a lo largo de la neuraxis, desde la médula espinal hasta la neocorteza (3, 4, 5).
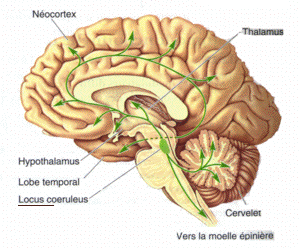
Composición neuroquímica del locus coeruleus
Posteriormente otras investigaciones demostraron que virtualmente todas las neuronas dentro del locus coeruleus de roedores y primates contenían DBH (6). Así, por lo tanto, estas neuronas contenían también norepinefrina como transmisor primario de LC.
Sin embargo, la identificación posterior de múltiples péptidos colocalizados dentro de las neuronas LC agregó nuevas dimensiones a lo que inicialmente parecía ser un sistema convencional de un transmisor. Así pues, aparte de la norepinefrina hay una variedad de neurotransmisores encontrados en las neuronas LC (7, 8):
- Vasopresina.
- Somatostatina.
- Neuropéptido.
- Encefalina.
- Neurotensina.
- Factor liberador de corticotropina.
- Galanina.
Actividad de las neuronas LC y función del LC
Las primeras investigaciones sobre el locus coeruleus determinaron que (9, 10):
- Las neuronas LC eran más activas durante la vigilia.
- Estas mismas neuronas presentan una actividad disminuida durante el sueño.
Trabajos posteriores demostraron que las neuronas LC también responden de forma fásica a estímulos salientes que producen respuestas de comportamiento (11, 12). Recientemente, otros estudios han encontrado que los patrones tónicos y fásicos de la actividad de el locus coeruleus interactúan.
Así pues, se entiende que las neuronas del locus coeruleus se disparan de forma tónica a velocidad moderada, pero se activan de forma fásica mediante señales relevantes para la tarea durante períodos de atención focalizada (2).
En contraste, la alta actividad tónica del locus coeruleus sin respuestas fásicas ocurre durante períodos de baja utilidad cuando la atención de la tarea se desvanece (2). Al parecer, estos y otros resultados llevaron a lateoría de la ganancia adaptativa (13).
La teoría de la ganancia adaptativa
Esta teoría, establecida por los autores Aston-Jones y Cohen en 2005, propone que las neuronas del locus coeruleus se activan de forma fásica en respuesta al resultado de la decisión. Ello ayuda a ejecutar respuestas conductuales adaptativas.
En contraste, la alta descarga del LC tónica en este modelo sirve para interrumpir el comportamiento de baja utilidad y aumentar la flexibilidad de comportamiento para que se puedan seguir estrategias de adaptación (2).
El locus coeruleus y su cambio con la edad
Los recuentos de neuronas LC cambian con la edad. Así, los investigadores que han puesto el ojo en este hecho han podido comprobar como se produce una clara disminución del número de neuronas LC con la edad (14).
La enfermedad de Alzheimer se origina en el LC
Una teoría reciente del desarrollo esporádico de la enfermedad Alzheimer propone que la patología más temprana asociada con el Alzheimer es la aparición de proteína tau anormal (hiperfosforilada) en algunas neuronas del locus coeruleus (15, 16).
En las neuronas sanas, la proteína tau estabiliza los microtúbulos. Estos proporcionan así un mecanismo de transporte dentro de las neuronas. Sin embargo, cuando está hiperfosforilado, tau pierde su función y puede eventualmente acumularse en ovillos neurofibrilares (14).
En general, se ha aprendido mucho desde las observaciones iniciales de Loizou sobre el locus coeruleus. Ahora que sabemos que está implicado también en patologías como el Alzheimer, parece obvia la necesidad de seguir investigando para conocer mejor esta estructura cerebral.
El locus coeruleus (LC) es uno de los núcleos más pequeños, pero más extensamente proyectados en el cerebro. Aparece citado por primera vez en el material publicado por Vicq-d’Azyr en 1786 (1). Hablamos de una estructura que se encuentra localizada en el tronco del encéfalo.
Así, esta estructura del sistema nervioso es conocida por conectar con muchas otras zonas del cerebro. De manera concreta, el locus coeruleus (LC) es una fuente importante de proyecciones de norepinefrina (NE) en todo el sistema nervioso central.
Así, en 1969 la revista Brain Research publica un artículo (Loizou, 1969) que arroja luz sobre esta estructura cerebral. El autor Loizou confirmó mediante su investigación que, como se pensaba, las proyecciones del LC estaban generalizadas y aparentemente difusas (2).
Anatomía del locus coeruleus
Tras la publicación de este trabajo de Loizou, hubo un esfuerzo considerable dedicado a obtener una caracterización más detallada del locus coeruleus y sus conexiones en el cerebro. Así, la investigación posterior a la publicación de la Brain Research se dedicó fundamentalmente a:
- El rastreo anterógrado y retrógrado del tracto.
- La tinción selectiva de las neuronas y fibras NE utilizando anticuerpos dirigidos contra la enzima sintética NE, dopamina-beta-hidroxilasa (DBH). Así, se confirmó la singularidad del locus coeruleus: se trataba de un grupo compacto de neuronas NE cuyas proyecciones se distribuyen ampliamente a lo largo de la neuraxis, desde la médula espinal hasta la neocorteza (3, 4, 5).

Composición neuroquímica del locus coeruleus
Posteriormente otras investigaciones demostraron que virtualmente todas las neuronas dentro del locus coeruleus de roedores y primates contenían DBH (6). Así, por lo tanto, estas neuronas contenían también norepinefrina como transmisor primario de LC.
Sin embargo, la identificación posterior de múltiples péptidos colocalizados dentro de las neuronas LC agregó nuevas dimensiones a lo que inicialmente parecía ser un sistema convencional de un transmisor. Así pues, aparte de la norepinefrina hay una variedad de neurotransmisores encontrados en las neuronas LC (7, 8):
- Vasopresina.
- Somatostatina.
- Neuropéptido.
- Encefalina.
- Neurotensina.
- Factor liberador de corticotropina.
- Galanina.
Actividad de las neuronas LC y función del LC
Las primeras investigaciones sobre el locus coeruleus determinaron que (9, 10):
- Las neuronas LC eran más activas durante la vigilia.
- Estas mismas neuronas presentan una actividad disminuida durante el sueño.
Trabajos posteriores demostraron que las neuronas LC también responden de forma fásica a estímulos salientes que producen respuestas de comportamiento (11, 12). Recientemente, otros estudios han encontrado que los patrones tónicos y fásicos de la actividad de el locus coeruleus interactúan.
Así pues, se entiende que las neuronas del locus coeruleus se disparan de forma tónica a velocidad moderada, pero se activan de forma fásica mediante señales relevantes para la tarea durante períodos de atención focalizada (2).
En contraste, la alta actividad tónica del locus coeruleus sin respuestas fásicas ocurre durante períodos de baja utilidad cuando la atención de la tarea se desvanece (2). Al parecer, estos y otros resultados llevaron a lateoría de la ganancia adaptativa (13).
La teoría de la ganancia adaptativa
Esta teoría, establecida por los autores Aston-Jones y Cohen en 2005, propone que las neuronas del locus coeruleus se activan de forma fásica en respuesta al resultado de la decisión. Ello ayuda a ejecutar respuestas conductuales adaptativas.
En contraste, la alta descarga del LC tónica en este modelo sirve para interrumpir el comportamiento de baja utilidad y aumentar la flexibilidad de comportamiento para que se puedan seguir estrategias de adaptación (2).

El locus coeruleus y su cambio con la edad
Los recuentos de neuronas LC cambian con la edad. Así, los investigadores que han puesto el ojo en este hecho han podido comprobar como se produce una clara disminución del número de neuronas LC con la edad (14).
La enfermedad de Alzheimer se origina en el LC
Una teoría reciente del desarrollo esporádico de la enfermedad Alzheimer propone que la patología más temprana asociada con el Alzheimer es la aparición de proteína tau anormal (hiperfosforilada) en algunas neuronas del locus coeruleus (15, 16).
En las neuronas sanas, la proteína tau estabiliza los microtúbulos. Estos proporcionan así un mecanismo de transporte dentro de las neuronas. Sin embargo, cuando está hiperfosforilado, tau pierde su función y puede eventualmente acumularse en ovillos neurofibrilares (14).
En general, se ha aprendido mucho desde las observaciones iniciales de Loizou sobre el locus coeruleus. Ahora que sabemos que está implicado también en patologías como el Alzheimer, parece obvia la necesidad de seguir investigando para conocer mejor esta estructura cerebral.
Todas las fuentes citadas fueron revisadas a profundidad por nuestro equipo, para asegurar su calidad, confiabilidad, vigencia y validez. La bibliografía de este artículo fue considerada confiable y de precisión académica o científica.
- Tubbs, R.S., Loukas, M., Shoja, M.M., Mortazavi, M.M., Cohen-Gadol, A.A., (2011). Félix Vicq d’Azyr (1746-1794): early founder of neuroanatomy and royal French physician., Child’s nervous system : ChNS : official journal of the International Society for Pediatric Neurosurgery. doi:10.1007/s00381-011-1424-y
-
Aston-Jones, G., & Waterhouse, B. (2016). Locus coeruleus: from global projection system to adaptive regulation of behavior. Brain research, 1645, 75-78.
-
Segal, M., & Landis, S. (1974). Afferents to the hippocampus of the rat studied with the method of retrograde transport of horseradish peroxidase. Brain Research, 78(1), 1-15.
-
Segal, M., & Landis, S. C. (1974). Afferents to the septal area of the rat studied with the method of retrograde axonal transport of horseradish peroxidase. Brain Research, 82(2), 263-268.
-
Swanson, L. W., & Hartman, B. K. (1975). The central adrenergic system. An immunofluorescence study of the location of cell bodies and their efferent connections in the rat utilizing dopamine‐B‐hydroxylase as a marker. Journal of Comparative Neurology, 163(4), 467-505.
-
Grzanna, R., & Molliver, M. E. (1980). The locus coeruleus in the rat: an immunohistochemical delineation. Neuroscience, 5(1), 21-40.6
-
Aston-Jones, G. (1994). The locus coeruleus, A5 and A7 noradrenergic cell groups. The rat nervous system.
-
Olpe, H. R., & Steinmann, M. (1991). Responses of locus coeruleus neurons to neuropeptides. In Progress in brain research (Vol. 88, pp. 241-248). Elsevier.
-
Aston-Jones, G., & Bloom, F. E. (1981). Activity of norepinephrine-containing locus coeruleus neurons in behaving rats anticipates fluctuations in the sleep-waking cycle. Journal of Neuroscience, 1(8), 876-886.
-
Hobson, J. A., McCarley, R. W., & Wyzinski, P. W. (1975). Sleep cycle oscillation: reciprocal discharge by two brainstem neuronal groups. Science, 189(4196), 55-58.
-
Aston-Jones, G. & Bloom, F. E. (1981). Nonrepinephrine-containing locus coeruleus neurons in behaving rats exhibit pronounced responses to non-noxious environmental stimuli. Journal of Neuroscience, 1(8), 887-900.
-
Hobson, J. A., McCarley, R. W., & Wyzinski, P. W. (1975). Sleep cycle oscillation: reciprocal discharge by two brainstem neuronal groups. Science, 189(4196), 55-58.
-
Aston-Jones, G., & Cohen, J. D. (2005). An integrative theory of locus coeruleus-norepinephrine function: adaptive gain and optimal performance. Annu. Rev. Neurosci., 28, 403-450.
-
Mather, M., & Harley, C. W. (2016). The locus coeruleus: Essential for maintaining cognitive function and the aging brain. Trends in cognitive sciences, 20(3), 214-226.
- Braak, H. and Del Tredici, K. (2015). Neuroanatomy and Pathology of Sporadic Alzheimer’s Disease, Springer International Publishing
- Braak, H. et al. (2011). Stages of the pathologic process in Alzheimer disease: age categories from 1 to 100 years. J. Neuropathol. Exp. Neurol. 70, 960–969
Este texto se ofrece únicamente con propósitos informativos y no reemplaza la consulta con un profesional. Ante dudas, consulta a tu especialista.







